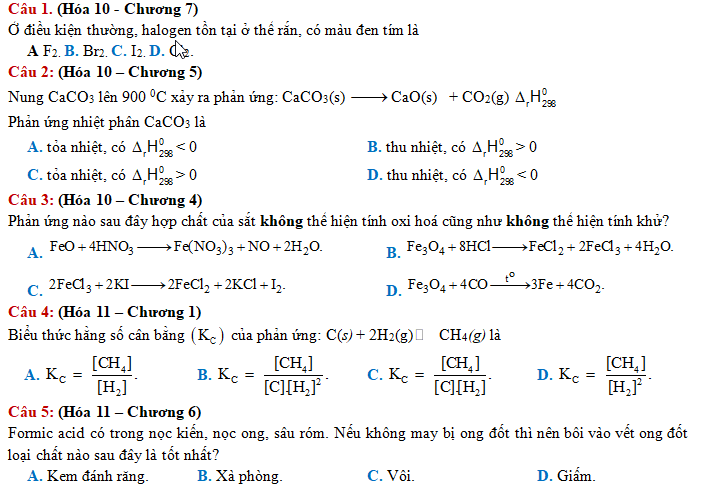Chào bạn, với vai trò là một chuyên gia giáo dục, tôi sẽ hướng dẫn bạn giải quyết các câu hỏi hóa học này một cách ngắn gọn, đi thẳng vào vấn đề và tuân thủ các yêu cầu định dạng đã cho.
### 📋 Tóm tắt đề bài
Đề bài yêu cầu giải 5 câu hỏi trắc nghiệm thuộc nhiều chủ đề khác nhau trong chương trình Hóa học phổ thông, cụ thể là:
1. **Câu 1 (Hóa 10 – Chương 7):** Nhận biết halogen tồn tại ở thể rắn, màu đen tím trong điều kiện thường.
2. **Câu 2 (Hóa 10 – Chương 5):** Xác định tính chất nhiệt của phản ứng nhiệt phân CaCO₃ (thu nhiệt hay tỏa nhiệt) và dấu của biến thiên entanpi chuẩn (Δr H°₂₉₈).
3. **Câu 3 (Hóa 10 – Chương 4):** Xác định phản ứng mà hợp chất của sắt không thể hiện tính oxi hóa lẫn tính khử.
4. **Câu 4 (Hóa 11 – Chương 1):** Viết biểu thức hằng số cân bằng nồng độ (K_C) cho một phản ứng dị thể.
5. **Câu 5 (Hóa 11 – Chương 6):** Chọn chất phù hợp để sơ cứu khi bị ong đốt (nọc ong chứa axit fomic).
### 💡 Hướng dẫn giải
**Câu 1:**
* **Hướng tiếp cận:** Dựa vào kiến thức về trạng thái và màu sắc của các halogen ở điều kiện thường.
* Flo (F₂) và Clo (Cl₂) là chất khí.
* Brom (Br₂) là chất lỏng, màu đỏ nâu.
* Iot (I₂) là chất rắn, màu đen tím, có khả năng thăng hoa.
* **Đáp án:** **C. I₂**
**Câu 2:**
* **Hướng tiếp cận:** Phản ứng nhiệt phân CaCO₃(s) → CaO(s) + CO₂(g) là một quá trình cần cung cấp năng lượng (nung) để xảy ra. Các phản ứng nhiệt phân thường là phản ứng **thu nhiệt**. Phản ứng thu nhiệt có biến thiên entanpi chuẩn **Δr H°₂₉₈ > 0**.
* **Đáp án:** **B. thu nhiệt, có Δr H°₂₉₈ > 0**
**Câu 3:**
* **Hướng tiếp cận:** Xác định số oxi hóa của nguyên tố sắt trong hợp chất ở cả chất phản ứng và sản phẩm. Hợp chất của sắt không thể hiện tính oxi hóa (không giảm số oxi hóa) và không thể hiện tính khử (không tăng số oxi hóa) khi số oxi hóa của sắt không thay đổi.
* A. FeO (+2) → Fe(NO₃)₃ (+3): Fe tăng số oxi hóa (khử).
* B. Fe₃O₄ (Fe có số oxi hóa trung bình +8/3, thực tế là hỗn hợp Fe(II) và Fe(III)) phản ứng với HCl tạo ra FeCl₂ (+2) và FeCl₃ (+3). Số oxi hóa của Fe trong Fe₃O₄ được bảo toàn trong các sản phẩm. Do đó, Fe₃O₄ **không** thể hiện tính oxi hóa cũng như tính khử.
* C. FeCl₃ (+3) → FeCl₂ (+2): Fe giảm số oxi hóa (oxi hóa).
* D. Fe₃O₄ (+8/3) → 3Fe (0): Fe giảm số oxi hóa (oxi hóa).
* **Đáp án:** **B. Fe₃O₄ + 8HCl → FeCl₂ + 2FeCl₃ + 4H₂O**
**Câu 4:**
* **Hướng tiếp cận:** Biểu thức hằng số cân bằng nồng độ (K_C) chỉ bao gồm nồng độ của các chất khí và chất tan trong dung dịch. Nồng độ của các chất rắn tinh khiết và chất lỏng tinh khiết được coi là không đổi và không đưa vào biểu thức K_C.
* Phản ứng: C(s) + 2H₂(g) ⇌ CH₄(g)
* Chất rắn C(s) không xuất hiện trong biểu thức K_C.
* K_C = [sản phẩm] / [chất phản ứng] = [CH₄] / [H₂]²
* **Đáp án:** **D. K_C = [CH₄] / [H₂]²**
**Câu 5:**
* **Hướng tiếp cận:** Nọc ong chứa axit fomic (HCOOH) là một axit. Để trung hòa axit và giảm đau, cần sử dụng một chất có tính bazơ (kiềm).
* A. Kem đánh răng: pH có thể thay đổi, không phải lựa chọn tối ưu cho việc trung hòa axit.
* B. Xà phòng: Có tính bazơ nhẹ, có thể trung hòa axit.
* C. Vôi: Thông thường là canxi hiđroxit (Ca(OH)₂), là một bazơ mạnh hơn xà phòng và rất hiệu quả trong việc trung hòa axit (ví dụ: dung dịch nước vôi trong hoặc bột nhão vôi tôi).
* D. Giấm: Chứa axit axetic (CH₃COOH), là axit, sẽ làm vết thương nặng hơn.
* **Lựa chọn tốt nhất:** Trong các lựa chọn, “vôi” (ở dạng an toàn như nước vôi trong) là chất bazơ có khả năng trung hòa axit hiệu quả nhất.
* **Đáp án:** **C. Vôi**